Девочки , часто вижу эту тему , но многие думают , что это не так опасно как резус конфликт , так вот , как мама троих деток могу сказать , что это важно ! С первым сыном всё обошлось в лёгкой форме , даже под лампочкой не лежал , второй родился сложно , гипоксия , и пошло поехало , желтушка на 3 сутки , обошлись лампой и капельницами , третьему досталось больше всего , мало того , что в роддоме лечились , так ещё и дома пришлось месяц специальный препарат пить !
Желтушная форма гемолитической болезни новорождённых
У меня отрицательная группа крови 0Rh(-) у мужа положительная 0Rh(+)
Срок 20 недель.
Анализы на антитела отрицательные.
Б. НЕ первая!
У меня очень высокая вероятность аллергии на белок ( аллергия на все другие белки) один раз сделали укол для иммунитета, был анафилактический шок:(((((
Анафилактический или анафилаксия — реакция немедленного типа, состояние резко повышенной чувствительности организма, развивающееся при повторном введении чужеродных белков и сывороток, медикаментов, при укусе . Одно из наиболее грозных осложнений , заканчивающееся примерно в 10-20 % случаев летально
Теперь я знаю:
1. – колоть его надо для профилактики, потому что неизвестно чей резус – фактор унаследует ребенок. (особенно если Б. не первая) – у меня НЕ ПЕРВАЯ! (анализ пока все же в норме ттт)
2. – если антитела начали повышаться колоть его уже нельзя, поэтому непосредственно перед уколом сдать анализ! (Мне врач сказал, что если не сделали в 28 недель, то это упущение мед. консультации. Этот укол обязателен, т.к. конфликт может возникнуть на 28-36 неделе беременности.)
3. – второй укол надо сделать в роддоме.
Резус-фактор — это (), который находится на поверхности красных кровяных телец (эритроцитов).
Около 85 % европейцев (99 % индейцев и азиатов) имеют резус-фактор и соответственно являются резус-положительными. Остальные же 15 % (7 % у африканцев), у которых его нет, — резус-отрицательный.
Резус-фактор играет важную роль в формировании так называемой новорожденных, вызываемой вследствие иммунизованной матери и эритроцитов плода.
Гемолитическая болезнь новорожденных (ГБН)— одна из наиболее частых причин желтухи у новорожденных. Болезнь развивается в результате иммунного конфликта из-за несовместимости крови матери и плода по группе крови или резус-фактору. В таких ситуациях факторы крови плода являются чужеродными для иммунной системы матери (так называемыми антигенами). Соответственно, иммунная система матери во время беременности реагирует на «чужаков», вырабатывая антитела, проникающие через плаценту к плоду и оказывающие повреждающее воздействие. В частности, антитела могут разрушить эритроциты ребенка, и тогда возникает гемолиз. Как результат, у такого новорожденного с первых дней и даже часов жизни развивается желтуха.
При благополучном течении беременности и обычной проницаемости плацентарного барьера антитела не вырабатываются, и гемолитической желтухи у малыша, как правило, не возникает. Однако риск ее развития повышается в несколько раз, если во время беременности у матери наблюдался гестоз или другие осложнения, был нарушен плацентарный барьер или нынешней беременности предшествовали другие. Во всех этих случаях иммунная система женщины уже сталкивалась с «враждебными» антигенами, а значит, ее организм реагирует привычно: антитела, вызывающие гемолиз у ребенка, вырабатываются в большем количестве.
Из трех форм гемолитической болезни новорожденного (анемической, желтушной и отечной) лишь симптомом желтушной является окрашивание кожи и слизистых в ярко-желтый цвет. Происходит это потому, что при гемолизе антитела матери, проникая через плаценту, разрушают эритроциты плода. Желтуха появляется сразу после родов, и даже околоплодные воды имеют желтую окраску.
Именно ГБН наиболее часто осложняется ядерной желтухой. Вот почему для профилактики этого состояния у детей всех женщин с резус-отрицательной кровью ставят на учет в женской консультации, а в течение беременности проверяют уровень антител и, при его повышении, вводят нейтрализующий антирезусный иммуноглобулин. Будущих рожениц госпитализируют в специализированный роддом за 2–3 недели до предполагаемой даты родов. Роды, как правило, стимулируют до 36-й недели беременности, так как позже увеличивается прохождение антител через плаценту к плоду и повышается вероятность развития тяжелых форм ГБН.
Гемолитические желтухи могут развиваться также при дефиците ферментативных систем эритроцитов, при нарушении структуры гемоглобина (например, при серповидно-клеточной анемии), при нарушении формы и структуры самого эритроцита (при анемии Минковского-Шоффара).
До сих пор НЕ ЗНАЮ:
1. какой конкретно колят белок и будет ли у меня аллергия на него.
2. где найти специалиста акушера – аллерголога и существуют ли такие? в аллерго – центре просто пишут – поливалентная аллергия. Про кровь и Б. они не очень понимают. В ЖК. не фига не знают про аллергии.
3. если будет все же аллергия сильно ли это повредит малышу и чем меня спасать
Кто знает, плиз пишите!!!!!!!
И первое разочарование.
Не, в общем-то, всё хорошо, моча, кровь. Но вот антитела на АВ0 (конфликт по группе крови)....
Отвечает Коноваленко Наталия Владимировна
гинеколог
Гемолитическая болезнь новорожденного проявляет себя  в первые часы, после рождения ребенка, в некоторых случаях она может быть выявлена еще внутриутробно. Основной причиной этого заболевания принято считать иммунологический конфликт (несовместимость крови плода и матери по антигенам эритроцитов).
в первые часы, после рождения ребенка, в некоторых случаях она может быть выявлена еще внутриутробно. Основной причиной этого заболевания принято считать иммунологический конфликт (несовместимость крови плода и матери по антигенам эритроцитов).
Гемолитическая болезнь новорожденного имеет такие формы:
1. Анемическая форма ГБН. Характеризуется бледностью кожных покровов, незначительным повышением билирубина в крови, увеличением селезенки и печени. Этот вид принято считать самым легким.
2. Желтушная форма ГБН. Появляется на 2 - 3 сутки, характеризуется увеличением печени и селезенки, повышенным билирубином, ребенок становится вялым и сонливым. Средняя форма тяжести заболевания.
3. Отечная форма ГБН. Развивается внутриутробно. Характеризуется гипоксией, тяжелой анемией, нарушением обмена веществ и сильной отечностью всех тканей. Может привести к самопроизвольному выкидышу или преждевременным родам. Самая тяжелая форма данного заболевания.
У детей первых дней жизни бывает, что кожа и слизистые оболочки приобретают желтоватый оттенок. Это происходит из-за нарушения билирубинового обмена, вследствие незрелости ферментных систем печени.
Собрала полезную информацию по резус-конфликту.
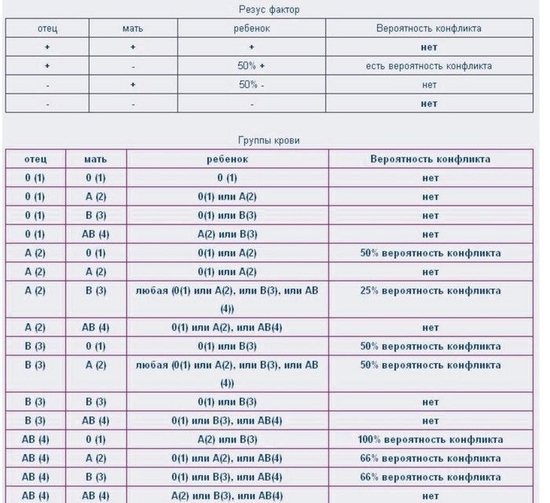
В женской консультации беременную обязательно проверяют на резус-фактор. Если он отрицательный, необходимо определить резусную принадлежность отца. При риске резус-конфликта (у отца - Rh+) кровь женщины неоднократно исследуется на наличие в ней антител к эритроцитам плода и их количество.
Отмечу, что совершенно необязательно при резус-несовместимой беременности разовьется резус-конфликт. Очень часто резус-конфликтная беременность протекает без каких-либо отрицательных последствий для плода, так как антитела в крови будущей мамы могут не вырабатываться совсем, или же вырабатываться в незначительном количестве, которое не представляет опасности для ребенка.
Каковы же факторы, которые могут поспособствовать выработке антител в организме будущей мамы?
Первый фактор способный спровоцировать выработку антител - это попадание крови малыша в кровоток мамы. Такая ситуация может возникнуть при родах, аборте или выкидыше. Также велика вероятность выработки антител при проведении амниоцентеза. Амниоцентез - это исследование, проводимое путем введения длинной иглы сквозь брюшную стенку в матку. Также, попадание «чужих» антител может произойти через плаценту. Усиливается опасность при наличии повышенной проницаемости плаценты, за счет инфекционных факторов, мелких травм, кровоизлияний.
Второй фактор риска может быть связан с тем, что «враждебные» антитела уже вырабатывались в организме женщины ранее, например, при переливании крови без учета резус - совместимости.
Третий фактор - это фактор неожиданности, ведь всегда существует вероятность того что антитела начнут вырабатываться в организме беременной женщины без каких-либо причин.
Если первая встреча организма с инородными телами уже произошла, то «память» организма неминуемо при повторном столкновении с угрожающими агентами осуществят выработку антител. Вот почему вероятность возникновения резус-конфликта при первой беременности сравнительно не высока и составляет всего лишь 10 %. Но, если не принять необходимых профилактических действий, то при возникновении второй беременности вероятность резус-конфликта существенно возрастет, так как в любом случае при родах происходит контакт резус-положительного ребенка с резус-отрицательной кровью его матери.

По уровню антител в крови будущей матери врач может определить возможное начало резус-конфликта и сделать выводы о предполагаемом резус-факторе у ребенка.
При первой беременности иммунная система будущей матери только «знакомится с чужаками» (Rh+ эритроцитами), антител вырабатывается немного и конфликт может не возникнуть. Однако в организме женщины остаются «клетки памяти», которые при последующих беременностях оперативно «организуют» быструю и мощную выработку антител против резус-фактора. Следовательно, риск поражения плода при каждой следующей беременности возрастает.
Поэтому сразу после родов определяют резус-фактор у младенца. Если он положительный, то матери не позднее 72 часов после родов вводят антирезусную сыворотку (антирезусный иммуноглобулин), которая предупредит развитие резус-конфликта при следующей беременности.
Такую же профилактику антирезусной сывороткой резус-отрицательные женщины должны проводить после внематочной беременности, аборта, выкидыша.
Вынашивание резус-конфликтной беременности
Судьба сыграла с вами злую шутку, случилось так, что вы падаете в группу риска. Не переживайте, любая проблема разрешима, нужно лишь составить план действий.
Первое что нужно сделать, это со всей ответственностью подойти к вопросу планирования беременности. А именно, стараться избегать ситуаций, способных спровоцировать резус-конфликт в будущем, среди них: аборт или выкидыш при положительном резус-факторе у плода. Если все-таки приведенные ситуации произошли, нужно как можно быстрее ввести специальный препарат, который предотвратит выработку резус - антител.
Получается так, что любое прерывание «положительной» беременности чревато в последующем серьезными последствиями для будущего ребенка, ведь если антитела уже однажды выработались, то они будут вырабатываться снова и снова при каждой резус-конфликтной беременности.
Когда беременность наступила, вам нужно постараться как можно быстрее встать на учет в женской консультации, и сразу же сосредоточить внимание вашего гинеколога на вашей особенности. Первая и, пожалуй, самая эффективная мера по обеспечению безопасности в таком случае - сдача крови на наличие в ней антител. Делать это нужно на протяжении всей беременности: до 32 недели - 1 раз в месяц, на 32-35 неделе 2 раза в месяц, на оставшемся сроке - еженедельно.
Если все идет хорошо, и антитела не обнаруживаются в крови, то на 28 неделе врач-гинеколог может порекомендовать сделать своеобразную «резус - прививку» - ввести антирезусный иммуноглобулин. Резус-прививка связывает попавшие в кровь матери эритроциты ребенка, таким образом, исключается возможность образования антител.
Если ситуация критична и титр антител существенно повышен, то необходима незамедлительная госпитализация будущей мамы и постоянный медицинский контроль ее состояния. Контроль состояния включает себя: отслеживание динамики титра антител в крови мамочки, данные исследования УЗИ, данные исследования околоплодных вод (амниоцентеза) или исследование пуповиной крови (кордоцентеза).

Если беременность достигла состояния доношенной, проводится плановое кесарево сечение. Если нет, то приходится прибегнуть к внутриутробному переливанию крови. Разрешение родов при прогрессирующем резус - конфликте, как правило, проводится путем кесарева сечения, делается это для того чтобы как можно скорее изолировать малыша от источника «опасных» антител.
При благоприятном разрешении беременности, то есть если антитела не выработались, а ребенок имеет положительный резус-фактор, вам обязательно должны будут сделать инъекцию антирезус - иммуноглобулина, для того чтобы уменьшить риск возникновения резус-конфликта при следующей беременности. Если выражаться точнее, то в роддоме должны сделать такую инъекцию, но для того что бы обезопасить и себя и будущего ребенка следует проконтролировать этот вопрос самостоятельно, договорившись заранее с вашим врачом. Для того чтобы быть полностью уверенной и исключить непредвиденные ситуации, лучше самостоятельно приобрести данный препарат и взять с собой в роддом.
Прикладывание малыша к груди при резус-конфликте.
«Когда у мамы отрицательный резус, а у отца положительный, кормить ребенка в pодзале можно, если беременность первая или после предыдущей беременности был сделан антиpезусный укол (анти-D иммунопpофилактика - Прим. автора), - поясняет консультант по ГВ Анна Ильина. - И вот почему: антитела в кpови (и в молоке) у такой мамы появляются только на второй-третий день после pодов, а если сделают анти-D укол, или ребенок окажется pезус-отpицательным, то антител не будет вообще».
«Хотелось бы объяснить позицию официальной медицины в плане раннего прикладывания к груди новорожденного с угрозой резус-конфликта, - отмечает врач- неонатолог Сергей Гончар. - Рекомендация выглядит достаточно категорично - первое свое кормление такой малыш должен получить в виде сцеженного донорского молока. Но, разумеется, модификации такого подхода вполне допустимы. И это очень здорово. Первая по счету беременность не является 100%-ой гарантией отсутствия в организме роженицы антирезус-антител. Иммунизация («активное знакомство» - Прим. автора) женщины резус-антигеном могла произойти намного раньше (при переливании крови, половых актах, проблемах с плацентой в ходе этой самой беременности и др. - Прим. автора).
Не дает полной гарантии безопасности и своевременно (не позже трех суток от момента родов) сделанная женщине инъекция антирезусного иммуноглобулина. Клетки памяти (особое семейство лимфоцитов) живут годами и способны быстро организовать бурный иммунный ответ на резус-антиген даже в том случае, если этих самых клеток остался минимум. Инъекция специфического иммуноглобулина сразу после родов уменьшает образование клеток памяти, но не может предотвратить выживание того самого минимума, который будет представлять опасность для малыша при следующей беременности».
Поэтому гарантию безопасности раннего прикладывания к груди малыша от резус-отрицательной мамы дает только один факт - отрицательная резус-принадлежность самого малыша. Теоретически это вполне возможно, а практически - проверяется в первые минуты после рождения ребенка.
Итак, если женщина резус-отрицательна, а ее супруг резус-положителен, то для того, чтобы аргументированно потребовать своего малыша для кормления прямо в родзале мамочке крайне желательно сделать следующее:
- если ваша беременность по счету первая, то все равно нельзя пренебрегать регулярным исследованием вашей крови на содержание (титр) антирезусных антител. Особенно если вам когда-либо переливали кровь;
- если беременность не первая, то такое исследование актуально вдвойне. При этом неважно, чем закончились предыдущие беременности - родами, выкидышами или абортами;
обязательно следите за титром этих антител даже в том случае, если вам вводили противорезусный иммуноглобулин после предыдущих родов (абортов, выкидышей)
- следуйте рекомендациям акушера-гинеколога, которые он дает по результатам обследования вашей крови;
попросите врачей сделать определение титра антител в последние сутки перед родами - по результатам этого исследования можно будет более или менее определенно судить о безопасности раннего прикладывания к груди. Если антитела имеются, то кормление уже таит потенциальную опасность;
попросите врача определить резус-принадлежность малыша cразу после рождения, не затягивая.
«Если ваш малыш резус-отрицателен - можете смело прикладывать его к груди (разумеется, если нет других противопоказаний), - подводит итог врач-неонатолог Сергей Гончар. - Если же он резус-положителен, и во время беременности (особенно непосредственно перед родами) у вас не обнаружены антирезус-антитела - приложить малыша к груди можно, но с разумной осторожностью. Хотя при первом своем кормлении новорожденный высасывает чаще всего очень небольшое количество молока, необходим регулярный контроль за уровнем билирубина, гемоглобина и эритроцитов в его крови. При указаниях на возможный резус-конфликт необходимо срочно перейти на вскармливание донорским молоком. И, наконец, если антирезус-антитела в крови матери обнаруживались во время беременности, раннее прикладывание к груди противопоказано.
Еще раз хотелось бы обратить внимание резус-отрицательных женщин - отсутствие в вашем организме вышеупомянутых антител не должно «доказываться» теоретическими выкладками - для этого существуют объективные методы исследования. И только с их помощью вы можете получить реальное представление о степени безопасности раннего прикладывания к груди вашего малыша».
А чем же опасен для ребенка резус-конфликт?
Попадая в кровоток плода, иммунные резус-антитела вступают в реакцию с его резус-положительными эритроцитами (реакция «антиген - антитело»), вследствие чего происходит разрушение (гемолиз) эритроцитов и развивается гемолитическая болезнь плода (ГБН). Разрушение эритроцитов приводит к развитию анемии (снижению количества гемоглобина) у плода, а также к повреждению его почек и головного мозга. Поскольку эритроциты непрерывно уничтожаются, печень и селезенка плода стараются ускорить выработку новых эритроцитов, при этом увеличиваясь в размерах. Основными проявлениями гемолитической болезни плода являются увеличение печени и селезенки, увеличение количества околоплодных вод, утолщение плаценты. Все эти признаки выявляются с помощью ультразвукового исследования во время беременности. В самых тяжелых случаях, когда печень и селезенка не справляются с нагрузкой, наступает сильное кислородное голодание, гемолитическая болезнь приводит к внутриутробной гибели плода в различные сроки беременности. Чаще всего резус-конфликт проявляется после рождения ребенка, чему способствует поступление большого количества антител в кровь младенца при нарушении целостности сосудов плаценты. Гемолитическая болезнь проявляется анемией и желтухой новорожденных.
В зависимости от степени тяжести гемолитической болезни различают несколько ее форм.
Анемическая форма.Наиболее доброкачественный вариант течения ГБН. Проявляется сразу после рождения или в течение 1-й недели жизни анемией, с которой связана бледность кожных покровов. Увеличиваются размеры печени и селезенки, есть небольшие изменения в результатах анализов. Общее состояние малютки нарушается мало, исход подобного течения заболевания благоприятный.
Желтушная форма.Это наиболее частая среднетяжелая форма ГБН. Основными ее проявлениями являются ранняя желтуха, анемия и увеличение размеров печени и селезенки. Состояние малыша ухудшается по мере накопления продукта распада гемоглобина - билирубина: кроха становится вялым, сонливым, у него угнетаются физиологические рефлексы, снижается мышечный тонус. На 3- 4-е сутки без лечения уровень билирубина может достигнуть критических цифр, и тогда возможно появление симптомов ядерной желтухи: ригидность затылочных мышц, когда малыш не может наклонить голову вперед (попытки привести подбородок к груди безуспешны, они сопровождаются плачем), судороги, широко открытые глаза, пронзительный крик. К концу 1 -й недели может развиться синдром застоя желчи: кожа приобретает зеленоватый оттенок, кал обесцвечивается, моча темнеет, в крови повышается содержание связанного билирубина. Желтушная форма ГБН сопровождается анемией.
Отечная форма- самый тяжелый вариант течения заболевания. При раннем развитии иммунологического конфликта может произойти выкидыш. При прогрессировании болезни массивный внутриутробный гемолиз - распад эритроцитов - приводит к тяжелой анемии, гипоксии (дефициту кислорода), нарушениям обмена веществ, снижению уровня белков в кровяном русле и отеку тканей. Плод рождается в крайне тяжелом состоянии. Ткани отечны, в полостях тела (грудной, брюшной) скапливается жидкость. Кожа резко бледная, лоснящаяся, желтуха выражена слабо. Такие новорожденные вялы, мышечный тонус у них резко снижен, рефлексы угнетены.
Печень и селезенка значительно увеличены, живот большой. Выражена сердечно-легочная недостаточность.
Лечение ГБН направлено в первую очередь на борьбу с высоким уровнем билирубина, выведение материнских антител и ликвидацию анемии. Среднетяжелые и тяжелые случаи подлежат оперативному лечению. К оперативным методам относятся заменное переливание крови (ЗПК) и гемосорбция.
ЗПК до сих пор остается незаменимым вмешательством при наиболее тяжелых формах ГБН, так как предупреждает развитие ядерной желтухи, при которой билирубином повреждаются ядра головного мозга плода, и восстанавливает количество форменных элементов крови. Операция ЗПК состоит в заборе крови новорожденного и переливании ему в пупочную вену донорской резус-отрицательной крови той же группы, что и кровь новорожденного). За одну операцию может заменяться до 70% крови малыша. Обычно переливают кровь в количестве 150 мл/кг массы тела ребенка. При выраженной анемии переливают препарат крови - эритроцитную массу. Операция ЗПК нередко проводится повторно, до 4-6 раз, если уровень билирубина вновь начинает достигать критических цифр.
Гемосорбция представляет собою метод извлечения из крови антител, билирубина и некоторых других токсических веществ. При этом кровь младенца забирают и пропускают через специальный аппарат, в котором кровь проходит через специальные фильтры. «Очищенная» кровь вливается малышу снова. Преимущества метода следующие: исключается риск передачи инфекций с донорской кровью, малышу не вводится чужеродный белок.
После оперативного лечения или в случае более легкого течения ГБН проводятся переливания растворов АЛЬБУМИНА, ГЛЮКОЗЫ, ГЕМОДЕЗА. При тяжелых формах болезни хороший эффект дает внутривенное введение ПРЕДНИЗОЛОНА в течение 4-7 дней. Кроме того, применяются те же методы, что и при транзиторной конъюгационной желтухе.
Весьма широкое применение нашел метод гипербарической оксигенации (ГБО). В барокамеру, куда помещают младенца, подается чистый увлажненный кислород. Этот метод позволяет заметно снижать уровень билирубина в крови, после него улучшается общее состояние, уменьшается воздействие билирубиновой интоксикации на мозг. Обычно проводится 2-6 сеансов, а в некоторых тяжелых случаях требуется проведение 11 -12 процедур.
И в настоящее время нельзя считать до конца решенным вопрос о возможности и целесообразности грудного вскармливания малышей при развитии ГБН. Одни специалисты считают его вполне безопасным, другие склоняются в пользу отмены грудного вскармливания в первую неделю жизни малютки, когда его желудочно-кишечный тракт наиболее проницаем для иммуноглобулинов и есть опасность дополнительного попадания материнских антител в кровяное русло младенца.
Из личного опыта могу посоветовать обсудить с врачом детским еще до рождения отсрочку прививки геппатита, т.к. она тяжелая, для ребнка с резус-конфликтом вообще отдельная консультация и граффик прививок важен.
Вторая и последующие беременности.
Если резус конфликт при первой беременности вас миновал, инъекция иммуноглобулина введена вовремя, то при вторая беременность для вас изначально ничем не будет отличаться от первой, т.е. вероятность развития резус конфликта при беременности по-прежнему останется на уровне 10%.
Для предотвращения резус-конфликта и гемолитической болезни во время второй беременности женщине проводят ряд инъекций, которые следует делать, как только обнаруживаются антигены в крови. В некоторых случаях антигены могут наблюдаться в крови уже с девятой недели беременности, что обязательно должно учитываться при выборе терапии матери. Большей опасности подвергаются те мамы, у которых присутствуют инфекционные процессы, нарушающие плацентарный барьер, небольшие кровоизлияния и травмирование плаценты.
Но в любом случае важно помнить: сам по себе факт возможности резус конфликта при беременности и даже наличия антител в крови - это не противопоказания к беременности и уж тем более не повод для ее прерывания. Просто такая беременность требует гораздо более ответственного и внимательного к себе отношения. Постарайтесь найти грамотного специалиста, которому вы полностью доверяете, и четко выполняйте все его рекомендации
Еще
Из всего что я читала на эту тему я поняла только что такие Б стоят на контроле. если антитела появляются, то проводят Амниоцентез и Кордоцентез, УЗИ дополнительные для контроля размера печени ребенка и многоводия у матери. Роды чаще всего проводят кесарево, что б снизить риск поражения. Часто вопрос о родах уже на 34 неделях поднимают. И рожать должны такие женщины в РД с детской реанимацией, т.к. если осложненная беременность, то вероятность ГМБ очень высока, а как правило тогда не редко необходимо переливание крови ребенку. Ну а из терапии, только если при билирубине что-то назначают, ну и капельницы.
Т.к. риск появления антител при Б есть, но есть и факт что не появятся, то стоит озаботится контролем титр и покупкой иммуноглобулина антирезусного, если к сроку его еще можно будет ввести.
Вот это из одной хорошей статьи:
Тактика ведения
Исследование крови на антирезусные антитела проводят всем беременным при первом обращении к врачу. Rh-отрицательным женщинам исследование повторяют на сроке 18-20 нед, а затем - ежемесячно. До 20-й недели беременности изоиммунизация развивается редко, обычно это происходит после 28-й недели беременности. Этим объясняются сроки введения анти-Rh0(D)-иммуноглобулина.
Rh-отрицательным женщинам, беременным Rh-положительным плодом, на сроке 28 нед вводят анти-Rh0(D)-иммуноглобулин. Этот препарат также обязательно назначают перед амниоцентезом. Риск изоиммунизации значительно зависит от метода родоразрешения. В родах дозу анти-Rh0(D)-иммуноглобулина подбирают в зависимости от результатов исследования мазка материнской крови, окрашенного по Клейхауэр-Бетке.
Тяжесть гемолитической болезни новорожденных.
В настоящее время окончательно не решено, влияет ли количество беременностей, сопровождавшихся изоиммунизацией, на тяжесть гемолитической болезни новорожденных. При первой беременности с изоиммунизацией водянка плода развивается примерно в 8% случаев. К сожалению, предсказать ее появление при последующих беременностях невозможно. Для оценки состояния и прогноза беременности у женщины с Rh-отрицательной кровью одного лишь определения титра антирезусных антител недостаточно.
Диаграмма Лили.
В 1961 г. Лили предложил специальный метод оценки данных спектрофотометрического исследования околоплодных вод, полученных путем амниоцентеза.
Установлено, что наиболее точно содержание в околоплодных водах билирубина и соответственно тяжесть гемолитической болезни отражает оптическая плотность околоплодных вод, определенная при прохождении света с длиной волны 450 нм. При построении своей диаграммы Лили использовал данные исследований, проведенных в разные сроки беременности у 101 женщины с изоиммунизацией.
На диаграмме выделяют три зоны соответственно трем степеням тяжести гемолитической болезни. Тяжелая гемолитическая болезнь соответствует зоне 3. Это состояние часто сопровождается водянкой плода. Ребенок, как правило, нежизнеспособен. Легкая гемолитическая болезнь соответствует зоне 1. В последние годы в диаграмму Лили были внесены некоторые изменения, в результате чего повысилась ее диагностическая и прогностическая точность.
Родоразрешение.
У 50-60% беременных с изоиммунизацией показания к амниоцентезу отсутствуют либо оптическая плотность околоплодных вод не превышает средних значений зоны 2 на диаграмме Лили. В таких случаях допускаются самостоятельные роды. Если на 35-37-й неделе беременности оптическая плотность соответствует верхней границе зоны 2 или имеет более высокие значения, на сроке 37-38 нед проводят родоразрешение. Предварительно определяют степень зрелости легких плода. При наличии водянки плода и сроке беременности более 34 нед (20% всех случаев водянки плода) родоразрешение проводят сразу, как только показатель оптической плотности достигнет верхней границы зоны 2. Предварительно определяют зрелость легких плода. Для ускорения созревания примерно за 48 ч до родов назначают кортикостероиды.
Лечение
Если риск недоношенности высок, родоразрешение откладывают и проводят внутриутробное лечение гемолитической болезни.
Внутриутробное переливание крови было предложено Лили в 1963 г. Он использовал метод внутрибрюшинного переливания. С появлением УЗИ стало возможным внутрисосудистое переливание крови: с 1981 г. с помощью фетоскопии, а с 1982 г. - путем кордоцентеза. Внутриутробное переливание крови - опасная процедура как для плода, так и для беременной, поэтому ее должен проводить опытный врач. Исследования показали, что большинство детей, перенесших внутриутробное переливание крови, растут и развиваются нормально. Отклонения отмечались в тех случаях, когда гемолитическая болезнь сочеталась с глубокой недоношенностью.
Анти-Rh0(D)-иммуноглобулин после родов вводят сразу, как только при исследовании пуповинной крови определен Rh-фактор. Если анти-Rh0(D)-иммуноглобулин не введен в течение 72 ч после родов, его непременно вводят не позднее двух недель после родов. При отсрочке эффективность профилактики снижается.
Дозу анти-Rh0(D)-иммуноглобулина рассчитывают в зависимости от объема фето-материнской трансфузии, которую оценивают при подсчете эритроцитов плода в мазке крови матери, окрашенном по Клейхауэр-Бетке. Если объем фето-материнской трансфузии не превысил 25 мл, вводят 0,3 мг анти-Rh0(D)-иммуноглобулина в/м, при объеме трансфузии 25-50 мл - 0,6 мг и т. д.
Расскажу нашу историю ГВ, так трудно начинавшуюся и закончившуюся хэппи эндом в 1,9 г.
Вот что я нашла про эту желтушку.
ЖЕЛТУХА НОВОРОЖДЕННЫХ, желтушка у новорожденных
Что такое желтуха у новорожденных?
Желтуха – это окрашивание кожи и слизистых оболочек в желтый цвет. Иногда желтушность кожи называют иктеричностью (от ikterоs - желтуха). Нередко родители слышат от лечащего врача, что у ребенка кожа и склеры глаз “иктеричны”, это значит, что они имеют желтушную окраску. Развитие желтухи связано с повышенным содержанием в крови особого вещества из группы желчных пигментов, которое называется билирубин (от bilis – желчь и rubin - красный). Этот красный желчный пигмент является главным пигментом желчи и продуктом обмена гемоглобина, именно он придает желчи характерный золотисто-желтый цвет. После отщепления молекулы железа от молекулы гемоглобина отщепляется и глобин (белковая часть вещества). Под влиянием окислителей происходит ряд биохимических реакций, в результате которых остается билирубин, который не содержит в своей молекуле белок. Такой билирубин называют непрямым, или свободным. Эта фракция билирубина попадает в плазму крови, “прикрепляется” к белку альбумину и в таком виде циркулирует в крови. Непрямой билирубин не растворяется в воде, токсичен и не проходит через почечный фильтр и почками не выделяется. В печеночной клетке к молекуле непрямого билирубина присоединяются две молекулы вещества, которое называется глюкуроновой кислотой, и образуется другая фракция билирубина – прямой билирубин, или связанный. Он не токсичен, растворяется в воде, проходит через почечный барьер и выделяется с мочой. Именно прямой билирубин хорошо проникает в ткани и обуславливает желтушное окрашивание кожи, склер, слизистых оболочек.
Различают 4 разновидности желтух: конъюгационные, гемолитические, механические (обтурационные) и печеночные (паренхиматозные). Конъюгационная (от лат. сonjugatio – соединение) желтуха связана с нарушением процессов превращения непрямого билирубина. Гемолитическая возникает вследствие интенсивного распада (гемолиза) эритроцитов. Обтурационная желтуха развивается в результате механического препятствия на пути оттока желчи в двенадцатиперстную кишку (при желчнокаменной болезни, при заболеваниях желчных путей). Печеночная (паренхиматозная) желтуха обусловлена поражением ткани печени при гепатите различной природы (вирусном, токсическом, реактивном).
Желтуха физиологическая (желтуха новорожденных) - транзиторная (временная) конъюгационная желтуха, возникающая у большинства здоровых новорожденных в первые дни жизни, вследствие того, что эритроциты плода содержат особый вид гемоглобина (гемоглобин F - фетальный) и эти эритроциты после рождения разрушаются. Кроме этого, у новорожденных имеется и дефицит специального белка, который обеспечивает перенос билирубина через мембраны печеночных клеток. Способствует избыточному накоплению билирубина запаздывание созревания ферментативных систем печени, участвующих в превращении непрямого билирубина в прямой. Еще один фактор, влияющий на скорость выведения билирубина из организма – это низкая выделительная способность печени у новорожденных детей.
Проявляется физиологическая желтуха новорожденных окрашиванием кожи в желтый цвет на 3-4-й день после рождения. Печень и селезенка не увеличиваются, признаков усиленного распада (гемолиза) эритроцитов и анемии нет. По мере улучшения работы системы выделения билирубина и исчезновения избыточных кровяных клеток из русла крови, желтуха исчезает (обычно через 1-2 недели) и не причиняет никакого вреда ребенку. При выраженной желтухе иногда используют внутривенное вливание растворов глюкозы, аскорбиновую кислоту, фенобарбитал, желчегонные средства для ускорения выведения билирубина.
Желтуха у недоношенных детей встречается чаще, чем у доношенных, она более выражена и держится более длительно – до 3-4 недель. Уровень прямого билирубина при этой форме желтухи достигает максимума на 5-6-й день жизни ребенка. В случае интенсивной желтухи дополнительно используют медикаментозные средства и фототерапию (терапию светом от специальной лампы). Под влиянием света происходит структурная изомеризация билирубина и образуется так называемый “люмирубин”, который имеет другой путь выведения, быстро проникает в желчь и мочу.
Выраженность повышения уровня билирубина в крови у недоношенных не зависит от массы тела при рождении, а находится в прямой зависимости от степени зрелости плода и наличия заболеваний матери в период беременности.
Редко встречается желтуха, вызываемая молоком матери (ее надо отличать от желтухи при грудном вскармливании), она встречается примерно у 1% вскармливаемых грудью новорожденных со значительными проявлениями желтухи. Появляется она после 1-й недели жизни ребенка. Предполагается, что эта форма желтухи связана с содержанием в молоке матери веществ из класса жирных кислот, которые угнетают функцию печеночных клеток ребенка и снижают активность ферментов, обеспечивающих “превращение” непрямого билирубина в прямой. Желтуха при грудном вскармливании развивается на 2-4-й день жизни, угасает на 3-4-й неделе, частота ее встречаемости - до 15 % случаев. При этом виде желтухи ребенка следует чаще кормить (можно больше 8 раз в сутки) грудным молоком, так как грудное вскармливание способствует более частому стулу и более быстрому выведению билирубина из организма. Так как у детей с повышенным уровнем билирубина часто повышенная сонливость, то их рекомендуют обязательно будить для кормления.
Прекращают грудное вскармливание у детей с желтухой только при некоторых наследственных заболеваниях, связанных с нарушением обмена веществ, например, при галактоземии.
К группе конъюгационных желтух относится конституциональная печеночная дисфункция (синдром Жильбера-Мейленграхта) – наследственное заболевание. Причиной нарушения билирубинового обмена при этой форме желтухи является изменение процессов захвата молекулы билирубина печеночной клеткой или нарушение связывания билирубина с глюкуроновой кислотой, что связано с наследственной неполноценностью ферментативных систем печени. По клинике синдром Жильбера очень сходен с транзиторной физиологической желтухой новорожденных. Печень и селезенка не увеличиваются, признаков повышенного распада эритроцитов и малокровия не наступает. Окраска кала и мочи нормальная. Лечение проводится симптоматическое. Прогноз благоприятный.
Желтуха у новорожденных может развиться при гипотиреозе - снижении функциональной активности щитовидной железы. Сочетается такая форма желтухи с другими признаками недостаточной выработки гормонов щитовидной железы: отечностью тканей, грубостью голоса, сухостью волос, повышением уровня холестерина крови, задержкой процессов окостенения и др. Возникает желтуха при гипотиреозе на 2-3-й день жизни, длится до 3-12 недель, а иногда и до 4-5 месяцев. Лечение проводят по рекомендации эндокринолога с использованием препаратов – гормонов щитовидной железы (тиреоидина).
Желтуха детей, родившихся у матерей с сахарным диабетом, связана с незрелостью печени ребенка, если у матери тяжелое течение сахарного диабета. При очень высоких показателях уровня билирубина проводят внутривенное вливание препаратов, способствующих более быстрому выведению билирубина из организма.
Желтуха у детей с пилоростенозом и обструкцией кишечника. Причиной повышения уровня непрямого билирубина крови при этом заболевании является обратное всасывание его из кишечника. При пилоростенозе увеличенный отдел желудка (привратник) может сдавливать общий желчный проток и нарушать желчеотделение (см. статью “Пилороспазм и пилоростеноз” в разделе Болезнь новорожденных). Лечение основного заболевания приводит к нормализации пигментного обмена и исчезновению желтухи.
Гемолитическая желтуха является проявлением повышенного разрушения эритроцитов ребенка. Наиболее часто она является симптомом гемолитической болезни новорожденного (ГБН), связанной с несовместимостью крови матери и плода по группе или резус-фактору. Развиваются гемолитические желтухи также при дефиците ферментативных систем эритроцитов, при нарушении структуры гемоглобина (например, при серповидно-клеточной анемии), при нарушении формы и структуры самого эритроцита (например, микросфероцитозе – анемии Минковского-Шоффара).
Патологическая желтуха проявляется в течение первых суток после рождения. Она развивается, когда чрезмерно быстро разрушается много эритроцитов. Если высвобождается очень много билирубина (медики говорят: "если уровень билирубина слишком высокий"), это может вызвать нарушения функции головного мозга. Такое состояние называют “ядерной желтухой” или “билирубиновой энцефалопатией”, так как при этой тяжелой форме желтухи новорожденных желчные пигменты и дегенеративные изменения обнаруживают в сером веществе головного мозга (особенно в ядрах ствола). Проявляется заболевание сонливостью, плохим сосанием, изменением рефлексов. Среди поздних проявлений - глухота, параличи, умственная отсталость.
Лечение зависит от причин развития гемолитической желтухи и нередко требует проведения заменного переливания крови.
Печеночная желтуха развивается при поражении печени вирусами, бактериями, простейшими (гепатит, сепсис, цитомегаловирусная инфекция и др.). При этом состоянии происходит накопление в крови непрямого и прямого билирубина. Кожа ребенка и слизистые оболочки окрашиваются в желтый цвет с зеленоватым оттенком, происходит увеличение печени, иногда и селезенки. Стул становится слабо окрашенным, моча приобретает более интенсивную окраску. В анализах крови обнаруживают повышение показателей активности печеночных ферментов. Лечение проводят комплексное, в зависимости от причин появления паренхиматозной желтухи.
При обтурационной (механической) желтухе желчные пути переполняются, разрываются и желчь поступает в кровяное русло. Происходит увеличение печени и селезенки, обесцвечивание кала и усиление окраски мочи. Эта форма желтухи может развиваться при кисте желчного протока, кольцевидной поджелудочной железе, атрезии (недоразвитии) желчных ходов, при сгущении желчи на фоне гемолитической болезни, при муковисцидозе и др. Лечение зависит от причин, вызвавших механическую желтуху. При ряде патологических состояний необходимо хирургическое вмешательство.
В настоящее время известно более 50 заболеваний, которые могут проявляться желтушным окрашиванием кожи у детей в период новорожденности. Поэтому длительное сохранение желтушного окрашивания кожи у новорожденного требует обязательного определения уровня общего билирубина и его фракций в сыворотке крови, показателей функции печени, общего анализа крови, ультразвукового исследования органов брюшной полости и консультации хирурга для уточнения причины желтухи и своевременного проведения лечения.
Сапа Ирина Юрьевна
Источник: www.detskiy-mir.com
Для начала - не путайте физиологическую желтушку новорожденного с желтухой.
Желтушка появляется практически у всех деток ещё в период нахождения в роддоме. В большинстве случаев она проходит сама через несколько дней.
Признаки - желтизна кожи ребенка и пожелтения белков глаз. Связано с повышением в крови билирубина (в норме до 26 мкмоль/л).
Есть много причин, препятствующих выводу билирубина из организма. Одна из причин - грудное молоко. Так же может быть из-за проблем с печенью, поэтому советуют делать узи брюшной полости, чтоб исключить этот вариант.
Чаще всего затянувшейся желтушке подвержены недоношенные дети.
Способы лечения:
- самое безобидное и очень хорошо действующее - нахождение новорожденного ребёнка на солнце. Если Вы родили летом - то в безветренную погоду как можно больше раскрывайте ребёнка - оголяйте руки, ноги, живот по возможности, лицо (многие мамы даже летом закутывают ребёнка в одеяло и частая ошибка - накрывают и всячески прячут лицо от солнца. В разумных пределах солнце ребёнку просто необходимо - витамин Д). Если погода не позволяет, то ложите ребёнка возле окна, чтоб на него попадал прямой солнечный свет (стекло, конечно, фильтрует лучи, но всё равно польза будет)
- вариант 2 - фактически то же самое солнце, только искусственное - кварцевая лампа. Делается процедура под наблюдением врача. Обычно достаточно 10 сеансов.
- медицинские препараты, способствующие выводу из организма билирубина. Для приема внутрь -глюкоза, активированый уголь. Капельницы - глюкоза (главное, чтоб потом у ребёнка не пришлось лечить нервную систему и грыжу от крика).
- кардинальный метод - переливание крови. Делается при очень больших показателях билирубина.
Опасность желтушки! Возможно развитие так называемой билирубиновой энцефалопатии - страдание мозга из-за токсического действия биллирубина.
Источник: http://www.malishok.info/article.php?ld=55
Привет девочки,хочу поделиться своей историей.У меня 1 отрицательная у мужа 4 положительная.2 ребенка родились отрицательные со 2 группой.Резус сенсабилизации не случилось соответственно,так как дети отрицательные.Но случился конфликт со вторым ребенком,а именно по группе крови ,сенсабилизация ко второй группе.Сын родился на 42 недели.У меня взя
ИЗОСЕРОЛОГИЧЕСКАЯ НЕСОВМЕСТИМОСТЬ КРОВИ МАТЕРИ И ПЛОДА
Основой изосерологической несовместимости крови матери и плода является неоднородность у них антигенных факторов эритроцитов крови, чаще по системе резус, реже по системе АВО. Вследствие проникновения факторов крови плода, обладающих антигенными свойствами, в кровоток матери, у которой они отсутствуют, в ее организме вырабатываются аллоиммунные антитела, которые через плаценту проникают к плоду, и в его организме возникает реакция антиген-антитело. Подобная реакция приводит к агглютинации и гемолизу эритроцитов плода, анемии, образованию непрямого билирубина - к гемолитической болезни плода и новорожденного (ГБП и ГБН).
При изосерологической несовместимости крови матери и плода заболевание может проявляться как во время беременности (ГБП), так и после рождения ребенка (ГБН).
Гемолитическая болезнь (синоним: эритробластоз) нередко является причиной смерти плода и новорожденного, повышенной заболеваемости в постнатальном периоде и последующие годы жизни.
Значительное снижение перинатальной смертности и заболеваемости детей было достигнуто благодаря применению заменного переливания крови новорожденным с ГБН, а также введением матери антирезус-иммуноглобулина (Rh IgG) после прерывания беременности любым путем (аборт, внематочная беременность, роды). Введенный Rh IgG связывает Rh-антигены, которые могут поступать в кровоток матери при прерывании беременности, и тем самым предотвращает выработку материнских антител и Rh-иммунзацию.
Издавна акушеры знали о заболеваниях (семейная желтуха,эритробластоз) новорожденных, сопровождающихся желтухой, нередко со смертельным исходом. Однако причина и патогенез гемолитической болезни стали известны только с 1940 г., когда американские ученые K.Landsteiner и A.Wienerобнаружили белковый фактор в эритроцитах, который обладал антигенными свойствами. Этими учеными в эксперименте было показано, что эритроциты обезьян (макака-резус) при введении кроликам вызывали у последних выработку антител. Реакция антиген-антитело(сыворотка иммунизированного кролика и эритроциты человека), выражающаяся в агглютинации, была обнаружена у 15 % людей. У остального населения подобный антиген, названный D-фактором, резус-фактором (Rh), содержится в эритроцитах, а также может быть в лейкоцитах, тромбоцитах и других клетках тканей. В последующем было доказано, что, помимо резус-фактора, в эритроцитах могут быть обнаружены и другие антигены, качественно отличающиеся друг от друга, - С (Rh') и Е (Rh"). Антиген С (Rh') содержится в крови 70 % людей, антиген Е (Rh") - 30 %. По существу кровь может считаться резус-отрицательной только в тех случаях, когда в ней отсутствуют все 3 разно видности резус-фактора. Резус-отрицательная кровь не лишена антигенных свойств, в ней обнаруживают связанные с эритроцитами аллели антигенов С, D, Е: с, d, e (система Нг), из них только антиген с может иметь значение в развитии иммуноконфликта в системе мать-плод.
Сложность системы резус обусловливается большим количеством мутаций каждого гена.
Наследование резус-антигенов определяется серией аллельных генов, расположенных на одной хромосоме, причем гены D и d, Сие, Еие находятся во взаимоисключающих отношениях. Присутствие D-антигена на эритроцитах обусловлено геном D, который имеет аллель d. Таким образом, возможны 3 генотипа: DD - гомозиготный, Dd - гетерозиготный и dd - гомозиготный. Все 3 гена одной хромосомы наследуются одновременно.
Гемолитическая болезнь плода и новорожденногоможет развиться также при несовместимости крови матери и плода по система АВО. Антигены А и В плода могут проникать во время беременности в кровоток матери, приводя к выработке иммунных а- и р-антител соответственно и развитию у плода реакции антиген-антитело (Аа, ВР). При этом иммунологическая несовместимость проявляется в том случае, если у матери 0(1) группа крови, а у плода - А(П) или В(Ш).
 Групповая несовместимость крови матери и плода встречается чаще (1 случай на 200-256 родов), но ГБП и ГБН протекают легче. Это объясняется защитной функцией околоплодных оболочек и околоплодных вод. Значительно реже ГБП и ГБН возникают при несовместимости крови матери и плода по другим эритроцитарным антигенам: Келл (К, к), Даффи (Fya-Fyb), Кидд (Ika), MNSs, PP, Лютеран (Lua-Lub), Льюис и др.
Групповая несовместимость крови матери и плода встречается чаще (1 случай на 200-256 родов), но ГБП и ГБН протекают легче. Это объясняется защитной функцией околоплодных оболочек и околоплодных вод. Значительно реже ГБП и ГБН возникают при несовместимости крови матери и плода по другим эритроцитарным антигенам: Келл (К, к), Даффи (Fya-Fyb), Кидд (Ika), MNSs, PP, Лютеран (Lua-Lub), Льюис и др.
Гемолитическая болезнь плода. Этиология и патогенез. ГБП и ГБН развиваются в том случае, если кровь матери резус-отрицательная, а кровь плода резус-положительная. Однако заболевание возможно также при резус-положительной крови матери и резус-отрицательной крови плода, при сенсибилизации к антигену с.
Как правило, ГБП и ГБН возникают после предшествующей резус-иммунизации, которая может наступить после попадания даже небольшого количества эритроцитов, содержащих Rh, в кровоток матери: переливание крови без учета резус-принадлежности, внутримышечное введение крови, а также попадание резус-положительных эритроцитов в кровоток матери во время предыдущей или настоящей беременности, сопровождающейся нарушением целости ворсин хориона или плаценты.
Резус-фактор формируется в ранние сроки беременности (по некоторым данным, начиная с 3-8-го дня беременности), эритроциты плода в крови беременных могут появляться при сроке 6-8 нед. Продолжительность циркуляции эритроцитов плода в кровотоке матери точно не установлена, однако известно, что аборты в ранние сроки гестации и внематочная беременность способствуют иммунизации - выработке антител в материнском организме. Роды особенно часто являются причиной попадания антигенов в кровоток матери с ее последующей сенсибилизацией. Опасность сенсибилизации увеличивается при оперативных родах, особенно во время кесарева сечения и ручного отделения плаценты. В меньшей степени вероятно попадание эритроцитов плода в кровоток матери в процессе беременности, но и это не исключено при наличии факторов, способствующих нарушению целости ворсин хориона и плаценты: амниоцентез, угроза прерывания беременности,предлежание плаценты, отслойка плаценты, наружный поворот плода, внутриутробная смерть плода. Даже небольшое количество антигена, попадающее в кровоток матери, может оказать выраженное сенсибилизирующее воздействие, вызвать выработку антител. Иммунизация может произойти и в процессе первой беременности, так как эритроциты плода могут попасть в кровоток матери, начиная с I триместра (6,7 %). Во II триместре гестации эритроциты плода обнаруживают у 15,9 %, в III - у 28,9 % беременных. Для иммунизации достаточно введения женщине с резус-отрицательной кровью 0,1 мл резус-положительной крови (этот факт доказан G.K.Cohen и соавт. в 1964 г. в экспериментах на добровольцах). Раз возникнув, антитела не исчезают, и чувствительность к повторному попаданию в организм резус-положительных эритроцитов велика.
После первой беременности иммунизируются 10 % женщин, но и при последующих беременностях возможна иммунизация такого же числа женщин, если она не произошла после первой беременности.
Тяжесть течения ГБП во многом зависит от вида антител, продуцируемых иммунной системой матери. Основную роль в развитии ГБП играют неполные антитела, относящиеся к IgG, которые легко проникают через плацентарный барьер. Полные антитела, относящиеся к IgM, имеют большую молекулярную массу и практически не проникают через плацентарный барьер.
Антирезус-антитела матери, попадая в кровоток плода, вызывают агглютинацию его эритроцитов или сначала их блокаду, а затем агглютинацию. В последующем независимо от варианта воздействия комплексы эритроцитов разрушаются, выделяется большое количество непрямого билирубина, возникают анемия и гипербилирубинемия. Если эритроциты не разрушаются в кровяном русле, то они накапливаются в селезенке и там подвергаются гемолизу под воздействием фагоцитов.
Обычно в том случае, если в организме появляется непрямой билирубин, он быстро переводится в прямой путем присоединения двух молекул глюкуроновой кислоты, вырабатываемой в печени. Прямой билирубин выводится почками. Непрямой билирубин плода может в определенном количестве выводиться трансплацентарно, а затем переходить в прямой в организме матери. Однако часть непрямого билирубина циркулирует в организме плода, чему способствует функциональная незрелость его печени. Кроме того, увеличение очагов эритропоэза в печени, расширение желчных протоков желчью, подвергшейся сгущению, приводят к изменению паренхимы печени и нарушению ее архитектоники. Последствиями этого являются уменьшение продукции протеинов в печени, гипопротеинемия,портальная гипертензия, асцит и генерализованные отеки. У плода при гемолитической болезни наряду с гипербилирубинемией возникают анемия и, следовательно, тканевая гипоксия с ацидозом. Непрямой билирубин является жирорастворимым, поэтому легко проникает в ткани, богатые липидами, подавляя ферментативные процессы. В связи с этим при гипербилирубинемии часто поражается мозговая ткань, особенно ядра головного мозга.
В зависимости от степени иммунизации ГБП может развиться в различные сроки беременности, иногда очень рано, начиная с 22-23 нед. При любом сроке беременности могут отмечаться наиболее тяжелые проявления заболевания -общая водянка, отечная форма ГБП. Чаще же заболевание возникает в первые часы и дни после рождения. В зависимости от степени тяжести заболевание может проявляться в анемической, желтушной форме и форме универсального отека. При всех формах выражена анемия.
При ГБП вследствие анемии, гипербилирубинемии, тканевой гипоксии, ацидоза нередко наблюдаются нарушения сердечной деятельности и состояния ЦНС. При ГБП беременность на всем протяжении может осложняться угрозой ее прерывания (поздний выкидыш, преждевременные роды).
Диагностика основывается на выявлении ряда признаков, связанных с иммунизацией матери, развитием гипербилирубинемии, анемии и гипоксии плода.
При определении тактики врача во время беременности, выборе способа и сроков родоразрешения, помимо выявления ГБП, очень важна оценка степени тяжести заболевания.
Важным признаком является обнаружение антител в крови матери. Этот диагностический тест не является абсолютным, так как антитела не исчезают после их выработки в организме матери, даже если в последующем не развивается заболевание плода или если у плода резус-отрицательная кровь. Однако в комплексе с другими признаками наличие антител позволяет с некоторой долей вероятности предположить ГБП.
Определенное значение имеет динамика титра антител. Титр антител отражает наибольшее разведение сыворотки крови (1:2, 1:4, 1:8, 1:16 и т.д.), при котором еще происходит гемолиз добавляемых к ней резус-положительных эритроцитов. Во время беременности титр антител может повышаться, несколько снижаться и колебаться. Нарастание титра антител не всегда определяется повышением степени иммунизации, иногда это объясняется попаданием их в кровяное русло из других клеток, а снижение - наоборот, связыванием их клетками. Тем не менее повышение титра антител, особенно значительное (на 3-4 порядка), учитывают как косвенный признак ухудшения течения ГБП.
Гипербилирубинемия и анемия являются одними из основных признаков ГБП, поэтому чрезвычайно важно определение степени их выраженности, о чем с известной долей вероятности можно судить по оптической плотности билирубина (ОПБ) в околоплодных водах. ОПБ повышается по мере увеличения концентрации билирубина, экскретируемого почками плода. Околоплодные воды получают путем пункции передней стенки живота, матки, околоплодных оболочек (см. Амниоцентез).
В околоплодных водах определяют ОПБ, титр антител, в случае необходимости - группу крови плода. При последнем амниоцентезе перед ро-доразрешением околоплодные воды исследуются на степень зрелости легких плода (пенный тест по методу Клеманса или определение соотношения содержания лецитина и сфингомиелина).
ОПБ устанавливают с помощью спектрофотометрии при длине волны 450 нм по отношению к дистиллированной воде. При этом нормальная величина билирубинового пика, как правило, не превышает 0,1. При ОПБ от 0,1 до 0,15 можно предположить наличие ГБП легкой степени. В том случае, если ОПБ составляет от 0,15 до 0;2, можно ожидать рождение ребенка со средней и тяжелой формой гемолитической болезни. ОПБ от 0,2 и выше, как правило, свидетельствует о развитии у плода тяжелой формы ГБП либо его внутриутробной гибели. При оценке ОПБ могут быть получены ложноположительные результаты вследствие попадания в иглу крови матери (при производстве амниоцентеза), мекония, мочи или асцитической жидкости плода. ОПБ может быть снижена при разведении билирубина большим количеством околоплодных вод при многоводии, что нередко наблюдается при ГБП. Более точно оценить тяжесть гемолитического процесса можно при исследовании ОПБ амниотической жидкости при различных длинах волн света - от 300 до 700 нм. В таких случаях вычисляют ЛЕ, наносят на график, разделенный на 3 зоны в зависимости от степени тяжести гипербилируби-немии и срока гестации. От того, в какую зону попадает установленное значение ОПБ, зависит дальнейшая тактика врача. Важную роль в диагностике ГБП имеет УЗИ, которое целесообразно проводить в следующие сроки беременности: 20-22, 24- 26, 30-32, 34-36 нед и непосредственно перед родоразрешением. УЗИ позволяет выявить изменения как плаценты, так и плода. В зависимости от степени тяжести заболевания наблюдается увеличение толщины плаценты (в норме она зависит от срока гестации, составляя в III триместре в среднем 34-36 мм). Превышение нормальной для срока гестации толщины плаценты на 0,5-1,0 см и более указывает на возможное заболевание плода, в связи с чем требуется провести повторное УЗИ. При отечной форме ГБП толщина плаценты может достигать 60-80 мм.
При гемолитической болезни УЗИ позволяет выявить у плода увеличение размеров печени и селезенки. Признаками отечной формы гемолитической болезни являются выраженная гепатоспленомегалия, асцит, многоводие. При выраженной водянке плода отмечаются, кроме того,кардиомегалия и перикардиальный выпот, гидроторакс, повышенная эхогенность кишечника вследствие отека его стенки, отек подкожной жировой клетчатки в области головы и конечностей плода. Дополнительными ультразвуковыми критериями оценки степени тяжести заболевания плода могут служить расширение вены пуповины (до 10 мм и более), повышенная скорость кровотока в нисходящей части аорты плода (скорость обратно пропорциональна содержанию гемоглобина у плода).
В связи с тем что плод при ГБП переносит гипоксию, степень выраженности которой увеличивается по мере нарастания тяжести заболевания, важно получить информацию о его функциональном состоянии. С этой целью проводят определение биофизического профиля по видоизмененнойшкале Vintzileos (1983). В отличие от маловодия, которое является неблагоприятным фактором у беременных без изосерологической несовместимости, при наличии таковой учитывают степень многоводия, а вместо степени зрелости плаценты - ее толщину. Остальные критерии шкалы (сердечная деятельность, дыхательные движения, двигательная активность, тонус) оцениваются по стандартной схеме (см. Дополнительные методы исследования. Определить наличие и степень тяжести ГБП возможно, проводя анализ крови плода, полученной из сосудов пуповины путем ее пункции (кордоцентез; см.Дополнительные методы исследования).
Кордоцентез позволяет произвести непосредственное исследование пуповинной крови с определением группы крови и резус-принадлежности плода, уровня гемоглобина, билирубина, сывороточного белка и гематокрита, прямой пробы Кумбса. Наиболее важным критерием ГБП считают гематокрит (Ht), который, с одной стороны, свидетельствует о степени гемолиза, а с другой, является показателем компенсаторных возможностей гемопоэза. Снижение Ht на 10-15 % указывает на тяжелую форму ГБП (в норме Ht до 26 нед составляет 35 %, позднее - от 38 до 44 %).
Ведение беременности и родов
У всех беременных при первом посещении врача определяют (или проверяют) группу и резус-принадлежность крови.
У беременных с группой крови 0(1) в том случае, если у мужа иная группа, необходимо исследовать кровь на наличие групповых иммунных антител. У пациенток с резус-отрицательной кровью следует, начиная с ранних сроков, проводить анализ крови на наличие антител и определения их титра: до 20 нед беременности 1 раз в месяц, в последующем 1 раз в 2 нед. Для установления предполагаемой резус-принадлежности плода выявляют наличие резус-фактора у отца. Необходимо также проведение непрямой реакции Кумбса, которая позволяет определить, какие антитела циркулируют в крови, связанные или свободные.
В отсутствие антител до 28 нед беременности многие исследователи рекомендуют беременным с резус-отрицательной кровью с профилактической целью внутримышечно вводить 300 мг Rh Ig, который может блокировать резус-антитела. Важно, чтобы препарат, содержащий антитела, не проходил через плаценту.
Определение состояния плода на основании результатов оценки биофизического профиля и УЗИ проводят еженедельно, начиная с 31-32 нед. У беременных группы высокого риска развития ГБП (наличие в анамнезе у беременных с резус-отрицательной кровью поздних выкидышей, преждевременных родов, мертворождений, ГБН, переливания крови без учета Rh-принадлежности). УЗИ нужно проводить ежедневно или с интервалом 1-2 дня.
С целью снижения сенсибилизации матери эритроцитами плода всем беременным с резус-отрицательной кровью даже в отсутствие у них резус-антител, а также при наличии АВО-сенсибилизации рекомендуется провести 3 курса неспецифической десенсибилизирующей терапии по 10-12 дней при сроке 10-12, 22-24, 32-34 нед. Женщины, у которых наблюдается осложненное течение беременности (угроза прерывания, токсикозы, гестозы), должны быть госпитализированы в отделение патологии беременных, где наряду с лечением основного заболевания проводят курс десенсибилизирующей терапии. Неспецифическая десенсибилизирующая терапия включает внутривенное введение 20 мл 40 % раствора глюкозы с 2 мл 5 % раствора аскорбиновой кислоты, 2 мл 1 % раствора сигетина и 100 мг кокарбоксилазы. Внутрь назначают рутин по 0,02 г 3 раза, теоникол по 0,15 г 3 раза или метионин по 0,25 г и кальция глюконат по 0,5 г 3 раза, препараты железа (ферроплекс по 1-2 драже 3 раза и др.), токоферола ацетат (витамин Е) по 1 капсуле. На ночь рекомендуется применять антигистаминные препараты (0,05 г димедрола, 0,025 г супрастина).
Беременным, в анамнезе которых имеются самопроизвольные выкидыши и роды плодом с отечной или тяжелой желтушной формой гемолитической болезни, при высоком титре резус-антител в специализированном учреждении можно проводить плазмаферез, заключающийся в изъятии у беременных определенного объема (250-300 мл) плазмы, содержащей антитела, с помощью различных аппаратов (РК-0,5 "АМИНКО" и др.). Замещение изъятой плазмы производят коллоидными, кристаллоидными и белковыми препаратами и одновременно возвращают в кровоток форменные элементы крови беременной. Плазмаферезвыполняют 1 раз в неделю под контролем титра антител, начиная с 23-24 нед беременности до родоразрешения; плазмаферез можно проводить и до беременности в качестве подготовки к ней.
С целью уменьшения степени резус-сенсибилизации осуществляют гемосорбцию с использованием активированного угля для сорбции свободных антител (см. рис.). Применение гемосорбции оправдано у беременных с крайне отягощенным акушерским анамнезом (повторные выкидыши, рождение мертвого ребенка). Наиболее оптимальным сроком начала проведения гемосорбции считается 20-24 нед беременности. Гемосорбцию проводят в стационаре. За один сеанс гемосорбции через гемосорбент перфузируется 8--12 л крови (2-3 ОЦК). Интервал между сеансами - 2 нед. Курс сорбционной терапии необходимо заканчивать за 1 нед до предполагаемого срока родоразрешения.
 Схема подключения устройства для проведения гемосорбции: 1 - катетеры, введенные в сосуды (в вену или в вену и артерию); 2 - трубчатая магистраль для забора крови; 3 - насос для прокачивания крови; 4 - пузырьковые камеры; 5 - устройство для подачи гепарина; 6 -манометры с делительными камерами, отделяющими их от непосредственного контакта с кровью; 7 - колонка с сорбентом; 8 - магнитный клапан для защиты пациента от воздушной эмболии; 9 - трубчатая магистраль для возврата крови. Стрелками показано направление движения крови по системе.
Схема подключения устройства для проведения гемосорбции: 1 - катетеры, введенные в сосуды (в вену или в вену и артерию); 2 - трубчатая магистраль для забора крови; 3 - насос для прокачивания крови; 4 - пузырьковые камеры; 5 - устройство для подачи гепарина; 6 -манометры с делительными камерами, отделяющими их от непосредственного контакта с кровью; 7 - колонка с сорбентом; 8 - магнитный клапан для защиты пациента от воздушной эмболии; 9 - трубчатая магистраль для возврата крови. Стрелками показано направление движения крови по системе.
В настоящее время широко проводят лечение ГБП путемвнутриматочных гемотрансфузий под контролем ультразвука. Гемотрансфузии плоду можно проводить начиная с 18 нед беременности. Внутриутробное переливание крови создает предпосылки для пролонгирования беременности. Существуют внутрибрюшной и внутрисосудистый способы гемотрансфузии. Техника внутрибрюшной трансфузии заключается в проколе брюшной стенки матери, стенки матки, брюшной стенки плода и введении в его брюшную полость одногруппной и резус-отрицательной эритроцитной массы, которая адсорбируется лимфатической системой и достигает сосудистой системы плода.
В последние годы предпочтение отдают внутрисосудистой гемотрансфузии плоду, показаниями к которой при резус-сенсибилизации являются выраженная анемия и гематокрит менее 30 %.
С целью проведения внутрисосудистой гемотрансфузии выполняют кордоцентез, при этом вену пуповины пунктируют в непосредственной близости от ее вхождения в плаценту. Проводник извлекают из иглы и производят забор крови для определения предтрансфузионного гематокрита плода. Эритроцитную массу медленно вводят через иглу, после чего забирают вторую пробу крови для определения конечного плодового гематокрита и оценки адекватности проведенной терапии. Для остановки движений плода, вследствие которых игла может быть вытолкнута им из вены пуповины, плоду вводят ардуан (пипекуроний) внутривенно или внутримышечно. Определение необходимости и времени проведения последующих гемотрансфузий плоду основывается на результатах УЗИ, посттрансфузионных показателях гемоглобина и гематокрита у плода.Проведение амниоцентеза после внутриутробной трансфузии не имеет смысла, так как амниотическая жидкость после этой процедуры обычно окрашена кровью, что может привести к ложноположительным результатам определения оптической плотности. Эффективность лечения тяжелых форм ГБП с помощью внутрисосудистого переливания крови составляет 85-91 %, при внутрибрюшном - 66 %.
Беременных, у которых отмечается резус-сенсибилизация, следует направлять в родильный дом при сроке беременности 34-36 нед, при АВ0-сенсибилизации - 36-37 нед для дополнительного обследования и решения вопроса о родоразрешении. При наличии ГБП необходимо досрочное родоразрешение, так как к концу беременности увеличивается поступление резус-антител к плоду. Оптимальные срок родоразрешения - 37-38 нед. беременности, так как при более раннем родоразрешении вследствие функциональной незрелости органов (особенно печени) гемолитическая болезнь протекает более тяжело, ребенок чаще страдает от респираторного дистресс-синдрома. Однако, если объективные данные свидетельствуют о выраженном страдании плода, если женщина имеет отягощенный акушерский анамнез, родоразрешение возможно и в более ранние сроки беременности. При этом необходимо провести мероприятия, направленные на ускорение созревания легких недоношенного плода. Назначают дексаметазон по 2 мг 4 раза в сутки за 2-3 дня до предполагаемых родов.
При выраженной отечной форме ГБП беременность прерывают при любом сроке. Если к моменту родоразрешения при УЗИ определяют очень большие размеры живота плода, целесообразно выпустить асцитическую жидкость путем прокола передней брюшной стенки матери, матки и передней стенки живота плода.
Как правило, родоразрешение проводят через естественные родовые пути. Кесарево сечение выполняют при наличии дополнительных акушерских осложнений (предлежание плаценты, неправильное положение плода, рубец на матке,выпадение пуповины и т.п.).
Родовозбуждение нужно начинать с создания глюкозо-витаминно-гормонально-кальциевого фона в течение 2-3 дней (в зависимости от состояния шейки матки). При готовности шейки к родам производят амниотомию. В случае, если родовая деятельность не разовьется, через 5-6 ч после амниотомии начинают родовозбуждение окситоцином или простагландинами по общепринятой методике.
В родах проводят тщательный контроль за состоянием плода, осуществляют профилактику гипоксии. Сразу после рождения ребенка его быстро отделяют от матери во избежание массивного попадания резус-антител в кровоток новорожденного. Из пуповины берут кровь для определения содержания билирубина, гемоглобина, группы крови ребенка, его резус-принадлежности. Проводят непрямую пробу Кумбса, позволяющую обнаружить эритроциты новорожденного, связанные с антителами (реакция агглютинации крови ребенка со специфической сывороткой Кумбса). Учитывая склонность плода и новорожденного с гемолитической болезнью к кровоизлияниям, следует бережно вести второй период родов. Целесообразны эпидуральная анестезия и рассечение промежности. При АВО-сенсибилизации ведение родов не имеет каких-либо особенностей.
В последующем при необходимости заменного переливания крови новорожденным с гемолитической болезнью используют пуповинные сосуды, поэтому скобку на пуповину не накладывают. Пуповину перевязывают на расстоянии 2-3 см от пупочного кольца.
Профилактика резус-сенсибилизации. Профилактические мероприятия заключаются в следующем: любое переливание крови производить с учетом резус-принадлежности крови реципиента и донора; необходимо сохранить первую беременность у женщин с резус-отрицательной кровью; профилактика и лечение осложнений беременности; проведение десенсибилизирующей терапии; осуществление специфической профилактики резус-сенсибилизации у женщин с резус-отрицательной кровью путем введения антирезус-иммуноглобулина после любого прерывания беременности.
Иммуноглобулин-антирезус вводят по одной дозе внутримышечно однократно. Родильнице указанную дозу назначают в течение 48 ч после родов, а лучше - 24 ч, при аборте - по окончании операции. После кесарева сечения и ручного отделения плаценты дозу препарата необходимо удвоить.
Важно произвести примерный расчет количества доз иммуноглобулина для родовспомогательных учреждений. Принимая во внимание данные литературы, следует считать, что из 1000 рожающих у 170 будет резус-отрицательная кровь. Из них у 100 женщин ребенок будет резус-положительным. Следовательно, на 1000 родов необходимо 100 доз препарата, если вводить его всем женщинам с резус-отрицательной кровью, родивших детей с резус-положительной кровью.
При неукоснительном выполнении методики специфической профилактики резус-сенсибилизации можно практически решить проблему резус-конфликтной беременности.
Девочки дорогие, те кто столкнулся с этой проблемой я хочу сюда выложить важную и нужную статью, уже столько людей пострадали от неграмотности врачей, они просто колечат жизни, но я хочу выложить полезную нужную и верную информацию, именно верную и правельную. Это статья очень квалифицированного доктора который занимаеться этой проблемой более 30 лет, который читает лекции на эту тему однако находяться умники врачи которые берут и назначают лечение беременных с резус -сеснсибилизацией, я хочу подчеркнуть лечения нет, не чего не поможет не снизить титр, не его убрать, а вот усугубить ситуацию можно, и так вот алгоритм правельного наблюдения за такими особенными беременными:
Современный алгоритм ведения беременности у пациенток с резус-сенсибилизацией. Профилактика